高考化学冲刺,化学平衡状态知识总结
2018-12-28 21:36:27三好网
1.可逆反应
(1)定义
在同一条件下既可以向正反应方向进行,同时又可以向逆反应方向进行的化学反应。
(2)特点
①二同:a.相同条件下;b.正、逆反应同时进行。
②一小:反应物与生成物同时存在;任一组分的转化率都小于(填“大于”或“小于”)100%。
(3)表示

2.化学平衡状态
(1)概念
一定条件下的可逆反应中,正反应速率与逆反应速率相等,反应体系中所有参加反应的物质的质量或浓度保持不变的状态。
(2)化学平衡的建立

(3)平衡特点

3.化学平衡状态的判断
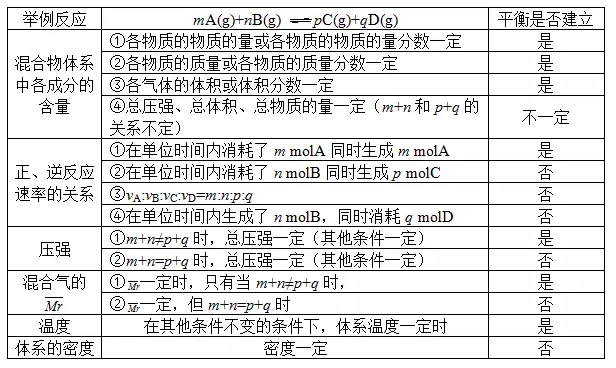
4.化学平衡常数
(1)定义
在一定温度下,当一个可逆反应达到化学平衡时,生成物浓度幂之积与反应物浓度幂之积的比值是一个常数,这个常数就是该反应的化学平衡常数,通常用符号K表示。
(2)表达式

(3)意义
①K值越大,说明正反应进行的程度越大,反应物的转化率越大。
②K只受温度影响,与反应物或生成物的浓度变化无关。
5.化学平衡常数的应用
(1)判断可逆反应是否达到平衡及不平衡时反应进行的方向
















